|
Article entré sur site en Janvier 2016 LES PRODIGES DE LA MEDECINE
PREDICTIVE Violaine
de MONTCLOS,Jérôme VINCENT, avec
Laurent Alexandre, Dominique Stoppa-Lyonnet, Olivier Caron, Arnold Munnich,
Mathilde Reynaud Référence
d’origine : Le Point, 17/10/13, N°2144
, A voir dans : http://www.lepoint.fr/sante/
|
|
|
Le choix d’Angelina
« Mes médecins ont
estimé à 87 % le risque que je développe un cancer du sein et à 50 % celui
des ovaires… Dès que j’ai connu ces
chiffres, j’ai décidé d’être proactive et minimiser les risques autant que
possible. » Dans une lettre parue le 14 mai 2013 dans le New York Times, Angelina Jolie déclarait
qu’elle était porteuse d’une anomalie génétique qui l’exposait au cancer dont
décéda sa mère. Et qu’elle avait subi, pour déjouer le sort, une mastectomie
bilatérale préventive. En révélant son choix chirurgical, qui réduisait dans
son cas la probabilité de développer un cancer du sein à 5 %, la sculpturale
actrice révélait au grand public le champ fascinant et encore balbutiant de
la médecine prédictive : lire dans nos gènes, pour mieux les déjouer,
nos maladies à venir. « La vie est pleine de défis. Ceux qui ne nous
font pas peur sont ceux que l’on peut surmonter et contrôler. » |
LES PRODIGES DE LA
MÉDECINE PRÉDICTIVE
Révolution.
Lire nos maladies futures
dans nos gênes, c’est déjà possible.
PAR
VIOLAINE DE MONTCLOS
Tout est là, dans une petite clé USB qui le quitte jamais. Laurent
Alexandre, énarque, médecin, ex-patron visionnaire et millionnaire du site
doctissimo.fr et directeur de DNA Vision, tient dans le creux d’une main le
séquençage de son propre génome : 21 000 gènes noyés dans les 3 milliards
de paires de bases chimiques qui forment son ADN. Une cartographie vertigineuse
de lui-même. Il a suffi d’un peu de salive et de quinze jours de patience, le
temps que met aujourd’hui un séquenceur haut débit pour trier les paires de
« bases », ces nucléotides désignés selon les lettres ATGC dont
l’ordre de succession définit notre identité génétique. La plupart des
combinaisons de ces quatre lettres sont communes à tous les hommes, mais
certaines, entre 2 et 4 millions, sont propres à chacun. Or ces variants sont
désormais repérés par notre informatique surpuissante et ils révèlent en quoi
nous sommes uniques. En termes d’apparence physique, bien sûr, mais aussi, dans
une certaine mesure, en termes de prédisposition à telle ou telle maladie.
Angoissante boule de cristal… « Le jour du séquençage n’a pas été le
plus jouissif de ma vie », dit l’industriel.
|
« Ce qui se passe est sans doute comparable à la découverte de l’Amérique. » |
Verdict : à la grande loterie génétique,
Laurent Alexandre n’a pas hérité, comme en atteste son épaisse chevelure, du
gène de la calvitie. Ni de celui qui prédispose à la maladie d’Alzheimzer,
résultat qu’il a longuement hésité à consulter. Mais il sait qu’il possède
trois variants qu’il qualifie de « graves », gènes mutés dont
la présence fait de lui un sujet un peu plus « à risque » que la
moyenne pour des maladies dont il ne révélera pas le nom. Mais qu’il s’emploie
désormais à déjouer. « Pour deux d’entre elles, je me fais dépister
régulièrement. Pour la troisième, j’ai un peu modifié ma façon de vivre. »
Quant aux millions d’autres variants, dont les milliers de potentiellement
pathogènes que les logiciels ont isolés pour lui, Laurent Alexandre est un peu
face à eux, comme tous les nouveaux industriels et chercheurs du génome,
comparable au Champollion des premiers jours devant la pierre de Rosette :
incapable d’interpréter. Quels gènes s’exprimeront ?
En fonction de quoi ? Selon quelle probabilité et quelles éventuelles
interactions ?
« Ce qui se passe est sans doute comparable, dans l’histoire de
l’humanité, à la découverte de l’Amérique. Mais il reste beaucoup à faire. Nous
savons séquencer le génome, mais nous ne savons en lire que 1 % des
informations. »
|
De 5 à 10 % c’est la part de cancers dits héréditaires. |
Nous
voilà donc, encore analphabètes ou presque, au seuil d’un nouveau continent
intérieur fait d’une succession infinie de lettres. Abasourdis d’y avoir
accosté si vite… En 1990, 6 pays, 20 centres de séquençage, des dizaines de
milliers d’experts décident d’allier leurs efforts pour parvenir à séquencer le
génome : le Projet Génome Humain voit le jour. La somme des données à
trier est monstrueuse, et certains spécialistes, à l’époque, estiment qu’il
faudra plusieurs siècles. Or, à peine treize ans plus tard, les progrès
exponentiels de l’informatique ont rencontré ceux de la génomique, et l’affaire
est plié :
le séquençage intégral est terminé. Et les coûts, rapidement, dégringolent :
3 milliard de dollars il y a dix ans, à peine 1 000 aujourd’hui, et la chute
continue : tous les six à douze mois, le prix est divisé par deux. En
2008, James Watson, découvreur de l’ADN, accepte que son génome – mis à part le
gène prédisposant à Alzheimer – soit publié dans la revue Nature. Il est
le second individu à être intégralement
séquencé. Cinq ans plus tard, plus d’un million de personnes dans le monde ont
fait établir leur cartographie génomique. La banalisation est en marche
|
Un individu sur 500 est porteur d’une mutation du gène BRCA 1 ou 2. |
|
162 c’est le nombre de maladies auxquelles vos gènes vous pré- disposent ou, à l’in- verse, vous rendent plus résistants, que la firme américaine 23andMe propose d’isoler à partir d’un simple kit salivaire.. |
Et la technique nous prend de vitesse, nous
précipitant dans des abîmes de questionnements éthiques et existentiels. Ainsi,
à peine le génome cartographié, nous voilà déjà capables – personne n’en avait
rêvé aussi vite – de distinguer grâce à un nouveau puissant algorithme les
séquences ADN d’une femme enceinte de celles de l’enfant qu’elle porte. Une
simple prise de sang et le génome intégral du fœtus est entre nos mains. Qu’en
faire ? En France, le Comité national d’éthique, saisi sur la question, a
donné en avril son feu vert pour que la trisomie 21 soit dépistée par
séquençage. Mais il a mis en garde les pouvoirs publics. « Dans un
avenir proche, il sera techniquement plus simple, et peut-être moins onéreux,
d’effectuer un séquençage entier du génome fœtal que de sélectionner des
régions d’intérêt et d’en réaliser un séquençage ciblé. » En
clair : non seulement nous saurons, encore une fois par simple prise de
sang, si l’individu à naître est atteint d’anomalies chromosomiques ou de
maladies génétiques graves – mucoviscidose, myopathie – mais nous saurons
aussi… tout le reste : prédisposition aux diabètes, cancers, maladies
neurodégénératives et autres innombrables variants encore difficiles à
interpréter. Qui pourra, alors que le tri d’embryons et de fœtus est déjà
largement admis dans nos sociétés, résister à la tentation eugénique ?
D’autant qu’il est déjà possible de se prémunir d’un certain nombre de risques
avant même la conception d’un enfant. Pour 99 euros,la société Counsyl, l’une
des innombrables entreprises, pour la plupart américaines,qui commercialisent
sur Internet ces tests interdits en France, propose de passer les gènes de
votre couple au crible et de déterminer si de votre union ne risque pas de
naître un enfant malade. « Si j’avais eu mon génome entre les mains
avant de devenir père, j’aurais certainement demandé à ma femme de se faire
séquencer aussi, admet Laurent Alexandre. Certains de mes variants,
s’ils avaient rencontré les mêmes chez mon épouse, auraient pu donner de graves
maladies chez nos enfants. L’avenir est à la “Gonomeetic” : demain,les
couples se feront aussi en fonction du profil génomique de chacun. »
|
|
Cartographié. Laurent Alexandre, chirurgien, dirige une
société spécialisée dans le séquençage. Il s’est lui-même fait séquencer. |
Déjouer le futur. Détourner l’épée de
Damoclès de sa cible. Allons-nous y gagner en maîtrise et en liberté ?
Lorsque la prédiction génétique concerne une maladie incurable, n’est-elle pas
plutôt un fardeau ? Les familles porteuses du gène de la terrifiante
chorée de Huntington connaissent bien ce questionnement obsédant : savoir
ou pas ? Alain, dont la mère et trois des frères et sœurs sont touchés, a
mis près de dix ans à se décider à passer le test, par bonheur négatif. « Je
l’ai fait, après des années à guetter avec angoisse les premiers signes de
huntington, lorsque mon propre fils a atteint l’âge de devenir père.Si je
m’étais avéré porteur, il était possible de faire un diagnostic
préimplantatoire au moment de la conception de ses enfants et d’éviter le pire
à la génération suivante. Mais, si cela n’avait concerné que moi, pour qui il
était de toute façon trop tard, je n’aurais peut-être pas voulu savoir. »
Sur
les 2 000 patientes que reçoit le professeur Stoppa-Lyonnet chaque année dans
son service d’oncogénétique de l’Institut Curie, quelques unes, qui ont fait le
test du gène BRCA, renoncent à venir chercher les résultats. En Occident, 1
individu sur 500 est porteur d’une mutation des gènes BRCA 1 ou 2, responsables
d’une forme familiale de cancer du sein ou des ovaires. Apprendre que l’on est
porteuse de l’un de ces gènes, c’est voir ses risques de développer ce cancer
augmenter dans des proportions vertigineuses. Pour Angelina Jolie, qui vient de
révéler au monde sa double mastectomie préventive,il était de 87 %. Mais Lara
Croft a réécrit l’histoire. « En France, environ 30 000 femmes âgées de
30 à 70 ans sont porteuses, mais moins de 15 000 sont identifiées, explique
le professeur Stoppa-Lyonnet. La difficulté est de savoir ce que la médecine
peut leur proposer une fois le diagnostic de prédisposition établi. À une femme
de 40 ans, en particulier si elle n’a pas eu d’enfants, il est difficile de
parler d’ablation des ovaires, mais les tests génétiques vont s’améliorer dans
un avenir proche et les risques s’affiner. Nous sommes encore au début de
l’oncogénétique. »
|
|
|
À qui appartiennent nos gènes ? 20 à 25 % des gènes humains ont déjà été
brevetés. Notamment les gènes BRCA1 et BRCA2, impliqués dans certains formes
de cancers du sein et des ovaires et brevetés par le laboratoire Myriad
Genetics, qui détenait depuis le milieu des années 90 le monopôle des tests
de dépistage aux États-Unis. D’où leur coût outre-Atlantique – 3 000 euros –,
d’ailleurs critiqué vertement par Angelina Jolie lorsque celle-ci a révélé sa
double mastectomie. En France, le professeur Dominique Stoppa-Lyonnet, chef
du service de génétique à l’Institut Curie et professeur de génétique à
l’université René-Descartes, est de ceux qui, avec l’Institut Curie,
l’Institut Gustave-Roussy, l’APHP et plusieurs sociétés européennes de
génétique, ont mené une fronde titanesque contre ce monopole. La bataille
juridique a duré plus de dix ans et, en juin 2013, la Cour suprême des
États-Unis a finalement invalidé les brevets de Myriad Genetics. « C’est
un formidable signal de facilitation de l’exploration du génome humain, se
réjouit le professeur Stoppa-Lyonnet. Les nouvelles technologies de
séquençage de l’ADN opèrent une rupture sur nos capacités d’analyse.
Cependant, s’il est maintenant très facile de générer de grandes quantités de
séquences d’ADN, l’interprétation des séquences, au moins pour une grande
partie d’entre elles, constituent un véritable défi. La décision de la Cour
suprême, qui, on l’espère, sera suivie par l’Office européen des brevets, va
permettre de le relever ■ |
Partout dans le monde, une course contre la
montre est lancée pour découvrir d’autres gènes, type BRCA1/2, ouvrant sur des
probabilités importantes de risques quantifiés. En particulier en matière de
pathologies cardiaques, dont on sait depuis longtemps que certaines sont liées
à des antécédents familiaux, donc probablement à des mutations de gènes. Un
véritable jackpot attend les découvreurs (voir encadré). Car la médecine
prédictive est d’abord un immense marché de l’angoisse qui peut rapporter gros
et sur lequel se ruent, depuis quelques années, un nombre considérable
d’entreprises du Net. Le problème : pour quelques centaines de mutations
donnant effectivement une forte probabilité de développer telle ou telle
maladie, la plupart de nos variants génétiques ne se traduisent, pour le
moment, que par des pourcentages infimes, non significatifs, impossibles à
analyser et néanmoins hautement anxiogènes. Notre génome, pour une part
écrasante, est à ce stade encore ininterprétable.
|
|
50 000 c’est le nombre d’habitants des îles Féroé, auxquels sera offert, dans les cinq années à venir, un séquençage complet
de leur génome. |
|
CERVEAUX L’usine à séquencer chinois le Beijing Genomic Institute, |
100 dollars d’ici à 2015, ce sera le prix du séquençage
complet du génome humain, qui coûtait 3 milliards de dollars |
Destin. « Savoir que vous avez 2,1 % de risques de plus que votre voisin
de développer un jour tel ou tel mal est une information dérisoire, sourit le professeur Sicard, président
d’honneur du comité d’éthique. Mais le marché s’est engouffré dans ce
dérisoire, le champ commercial est immense, et la médecine dite prédictive
prend le pas sur la préventive. Pourtant, si vous fumez 60 paquets de cigarettes
par mois, je peux vous prédire mieux que n’importe quel séquençage que vous
développerez une bronchopathie précoce… Mais modifier un comportement, se
préserver du soleil ou de la cigarette, bien que moins onéreux, semble beaucoup
moins attractif, pour nos contemporains, qu’un chiffre fondé sur des éléments
techniques. Aussi aléatoire soit ce chiffre… » Étrange arithmétique
personnelle, souvent irrationnelle, du risque individuel face à la maladie.
Comme s’il était toujours possible d’échapper aux cohortes de fumeurs dont on
sait pourtant à coup sûr qu’ils tomberont malades, mais pas à ce tout petit
pourcentage qui nous distingue génétiquement, face à tel ou tel mal, de notre
voisin. Comme si, au fond, comme l’avait prophétisé le généticien François
Jacob, nous préférions en remettre à nos gènes et leur demander ce que nous
réclamions autrefois aux dieux : lire notre destin à l’avance. La médecine
prédictive en est à son genèse. Et a, on peut le prophétiser, de beaux jours
devant elle ■
|
SAVOIR OU PAS ? Une mutation du gène ApoE peut signer une
prédisposition à la maladie d’Alzheimer quinze fois supérieure à la moyenne.
Sachant que la maladie ne bénéficie pour le moment d’aucun traitement, une
équipe de l’université de Boston a testé 162 individus et a révélé 53 d’entre
eux, avec toutes les précautions possibles, qu’ils étaient porteurs de la
mutation. Au lieu des réactions de paniques attendues, les malchanceux,
suivis régulièrement par des thérapeutes, ont pour l’essentiel fait face à la
mauvaise nouvelle et ont changé de mode de vie. |
|
CHER WATSON Le Nobel James Watson, découvreur de l’AND,
est le premier individu à avoir fait séquencer intégralement son génome avec
un séquenceur haut débit nouvelle génération. Les résultats furent publiés en
2008 dans la revue « Nature ». tout son génome… sauf le gène
prédisposant à la maladie d’Alzheimer, verdict qu’il refusait de connaître. |
AU BERCEAU Le séquençage du génome à la naissance
peut-il changer notre destin ? Pour répondre à cette question, les
États-Unis viennent d’établir un programme massif de séquençage intégral de
nouveau-nés. 25 millions de dollars ont été trouvés, et quatre programmes de
recherche menés sur cinq ans sont désormais lancés. Le recrutement des futurs
bébés et de leurs familles devrait commencer en 2004. |
||||
|
|
|
|||||
|
VERS UNE MÉDECINE PERSONNALISÉE L’individu réagit aux traitements en fonction, entre autres, de son
profil génétique, et certains médicaments sont d’ores et déjà prescrits et/ou
dosés après que le patient eut été soumis à des tests génétiques. La première
conséquence des progrès de la génomique est donc de nous projeter vers une
médecine « sur mesure » plus efficace. Le séquençage du génome a aussi des
applications dans le traitement du cancer. Car un cancer résulte presque
toujours d’altérations de l’ADN. Or le séquençage des tumeurs révèle que les
mutations de gènes sont multiples, complexes et surtout propres à chaque
patient. Connaître entièrement l’ADN d’une tumeur permet donc d’adapter
précisément le traitement à chaque malade.Une révolution. |
|
|||||
|
|
Olivier Caron, responsable de la consultation d’oncogénétique de l’Institut Gustave-Roussy. |
Olivier Caron : « chiffrer le
risque »
ADN. L’oncogénéticien s’attaque à l’hérédité de certains cancers.
Le Point : Quelle est la part de cancers dus à une mutation génétique
héréditaire ?
Olivier Caron : Pour le
moment, de 5 à 10 %. Mais je préfère parler d’anomalie que de mutation. Nous
avons tous globalement les mêmes gènes, avec des variations individuelles.
Certaines sont sans conséquences ; d’autres, en revanche, impliquent que
le gène ne joue pas le rôle qu’il est censé de jouer et que la probabilité de
développer tel ou tel cancer augmente de façon importante. Sont concernées
certaines formes familiales de cancers de sein, des ovaires, du colon, de la
thyroïde ou des glandes surrénales. Mais l’oncogénétique est une discipline
très jeune, il reste beaucoup de choses à découvrir. Par exemple, préciser la
probabilité pour chaque individu. Et trouver d’autres gènes responsables dans
ces cancers-là, et peut-être dans d’autres tumeurs.
À qui s’adresse votre consultation ?
On ne teste pas les individus à l’aveugle. Les deux critères évoquant
une anomalie génétique sont le nombre de cancers dans une même famille et l’âge
précoce de survenue de ce cancer. Une fois le gène isolé chez celui que l’on
appelle le cas « index », c’est-à-dire la personne malade ou qui a
été malade, on propose aux membres de sa famille de se faire tester, mais c’est
évidemment leur stricte liberté de refuser. On informe les enfants et les
frères et sœurs qu’ils ont un risque sur deux d’être porteurs du gène et, s’ils
se font tester, nous sommes capables de chiffrer leur risque de développer le
cancer. Mais ce sont des moyennes statistiques qu’on ne donne que si la
personne les demande, toujours en les commentant.

Vous leur faites donc une forme de prédiction.
Même si c’est un peu jouer sur des mots, je réfute ce terme de
prédiction. On ne peut accepter de faire de tests de ce type que si l’on a une
prise sur le risque. Ce n’est pas une fin en soi de savoir si l’on est porteur
ou pas de la prédisposition familiale ; ce qui compte, c’est ce que cela
va changer à la prise en charge de l’individu : surveillance accrue et,
dans certains cas, chirurgie préventive.
Comment procédez-vous pour déceler l’anomalie ?
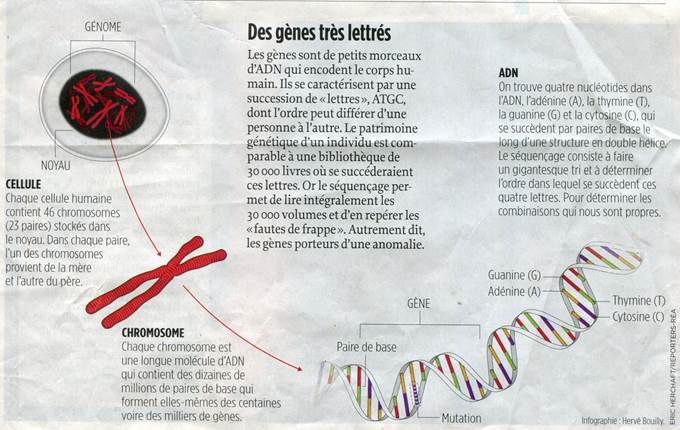
On extrait l’ADN à partir d’une prise de sang. Mais on n’explore pas
tout. Il faut se présenter le patrimoine génétique comme une bibliothèque qui
comporterait de 25 000 à 30 000 volumes. Lorsque l’on sait quels gènes
chercher, par exemple les gènes BRCA1 et 2 impliqués dans le cancer du sein et
des ovaires, on se contente de passer au crible deux de ces volumes, et l’on y
cherche ce que l’on pourrait comparer à une faute de frappe par rapport au
texte d’origine. Une seule lettre différente peut suffire à faire augmenter les
probabilités de cancer, mais ce peut être un chapitre entier qui a disparu.
L’analogie avec un texte est assez réaliste, car ce sont bien des lettres que
nous lisons, les fameuses lettres ATGC.
Et, avec le séquençage du génome, on sait désormais lire la
bibliothèque entière !
Oui, nous assistons à une explosion technologique, les outils de
séquençage sont devenus extrêmement performants. Au point qu’un séquençage
intégral peut aujourd’hui aller plus vite que l’exploration d’un gène ciblé.
Cela ouvre un champ d’exploration fascinant et qui donne le vertige. Mais
attention, on sait lire toute la bibliothèque, on sait y déceler les dizaines
de milliers de fautes de frappe, mais c’est une information brute que nous
sommes encore loin de savoir interpréter. En tant que médecin, je n’ai pas
envie, du moins à ce stade, d’amener les patients vers le séquençage intégral.
Mais, du côté de la recherche, ces nouvelles technologies nous offrent des
outils d’une performance sans précédent… ■
PROPOS RECUEILLIS PAR VIOLAINE DE MONTCLOS
|
|
|
Arnold Munnich, responsable du département de génétique de
l’hôpital Necker-Enfants malades à Paris. |
Arnold Munnich : « La médecine, ce n’est pas le tiercé »
Mise au point.
Le généticien met en garde contre les dérives de la médecine prédictive.
Le Point : Vous êtes un des pionniers français du conseil génétique. Un million
de personnes dans le monde ont fait établir une cartographie génétique. La
banalisation est en marche. Qu’en pensez-vous ?
Arnold Munnich : Cela me
gène. J’ai le souci des patients. En tant que médecin, je suis inquiet.
Aujourd’hui, on ânonne le génome. Nous savons en partie le lire, mais nous le
comprenons pas. Nous sommes devant une masse de signes et nous nous demandons
ce que c’est. Il y a un certain nombre de choses que nous savons
identifier : la normalité. Mais imputer en toute rigueur l’anomalie d’un
gène ou d’une séquence génétique est difficile. C’est cela qui m’inquiète,
aller dire des choses aux gens qui ne sont pas vérifiées. Cette plaisanterie a
assez duré.
Le Comité national d’éthique a donné son feu vert pour que la trisomie
21 soit dépistée par séquençage, une simple prise de sang chez la femme
enceinte permettant de connaître le génome du bébé qu’elle porte. Êtes-vous
d’accord ?
C’est un projet de recherche pour évaluer une pratique qui n’est pas
encore en place.
Tout le monde a droit de chercher. Ça se fait d’ailleurs à l’hôpital Necker
dans ce cadre, avec des professionnels de très grande qualité. J’ai toute
confiance. Nous verrons l’issue de cette recherche. Quels seront les rapports
entre les avantages et les inconvénients, ou le coût et l’efficacité, de cette
voie en regard du dépistage mis en œuvre aujourd’hui ? Nul le sait. Tout
ce qui est techniquement possible n’est pas économiquement faisable ni
éthiquement supportable. Si nous nous tenons au seul dépistage de la trisomie
21 et pas à d’autres maladies, et si c’est fait dans de parfaites conditions
médicales, d’explications aux personnes, je pense que nous sommes simplement
dans l’optimisation d’une procédure qui existe déjà aujourd’hui, qui est
acceptée et qui peut avoir des ratés.
Quelles sont, selon vous, les promesses de la médecine
prédictive ?
Je n’en vois pratiquement pas. C’est peut-être mon ignorance. Comme nos
compatriotes ne supportent pas le doute, l’incertitude, je cerne bien qu’il
existe un terrain très favorable à un gigantesque marché lucratif pour des gens
peu scrupuleux. Ce qu’on peut dépister, ou qui pourrait l’être, n’est pas
forcément assorti de mesures préventives ou thérapeutiques. Dans ces
conditions, ce n’est pas une médecine prédictive, mais une médecine
malédictive. Quand on examine en détail ce qui est proposé, deux éléments de
réserve scientifiques apparaissent clairement. Les résultats valent en
population, mais pas pour un individu. Et ils sont exprimés comme la cote des
chevaux, en termes de chance – non pas de gagner, mais de perdre. Or la
médecine, ce n’est ni la loterie ni le tiercé.
Néanmoins, nous ne pouvons pas condamner la médecine prédictive. Elle
va peut-être nous permettre de sélectionner des médicaments plus efficaces et
mieux supportés pour chaque patient en fonction de sa constitution génétique.
Peut-être existera-t-il à l’avenir une belle science de
pharmacogénétique ? Mais nous n’y sommes pas, nous en sommes même encore
très loin. La médecine prédictive est intéressante, mais elle doit être
considérée avec la plus grande prudence au niveau individuel.
Quel conseil donneriez-vous à quelqu’un voulant acheter à une société
étrangère une prestation pour faire cartographier son génome ?
Franchement, cela frise l’abus de confiance. Je vais vous raconter une
histoire. J’ai un collègue, un généticien américain, qui me dit un jour qu’il a
fait tester son génome. D’après les résultats, il aurait dû être mort. Vous
voyez le sérieux. Je suis là pour protéger les patients. Ce qui est proposé
aujourd’hui les expose à davantage de souffrances.
Mais la ligne rouge n’est-elle pas déjà dépassée ?
Non. Bien sûr, les Français consultent Internet et, s’ils font tester
leur génome par cette voie, ils vont recevoir un listing incompréhensible. Mais
ils sont intelligents et ils disposent d’une bonne médecine. À nous de prendre
le temps de leur expliquer. L’opinion a besoin d’être éclairée. Dans notre pays
comme dans d’autres, il existe des garde-fous. Nous ne sommes pas aux
États-Unis ni aux Pays-Bas. Ce n’est pas le côté lucratif qui doit guider la
prescription d’un test, un bon médecin est celui qui prescrit le juste test ■
PROPOS RECUEILIS PAR JÉRÔME VINCENT
|
Ce qui est autorisé, ce qui est interdit La législation est assez stricte en France
depuis l’adoption des lois bioéthiques en 1994, qui ont été révisées en 2011.
Les tests génétiques sont autorisés et peuvent être effectués uniquement dans
une visée médicale, judiciaire ou dans le cadre d’une recherche scientifique,
et ils sont nécessairement prescrits par un médecin. La réalisation des tests
est également strictement encadrée. Au préalable, il est impératif d’informer
largement la personne sur les avantages, les risques, L’utilisation des tests génétiques dans le
domaine des assurances est exclue. Il n’a été prévu aucune mesure
d’encadrement (interdiction, limitation, régulation) des tests sur Internet,
étant donné la facilité avec laquelle il est possible d’en obtenir un… ■ J.V. |
|
Mathilde Reynaudi, chargée de mission au Commissariat général
à la stratégie et à la prospective. Auteur d’un rapport en 2012. |
|
Mathilde Reynaudi : « Une
révolution dans les soins »
Le Point : Quelle est la réalité de la médecine prédictive à ce jour ?
Mathilde Reynaudi* : Les progrès vont vite. Le séquençage du génome humain, terminé en 2003,
a coûté 3 milliards de dollars. Il y a un an, un test très simple, accessible à
tous par Internet – on l’achète, on envoie son prélèvement de salive par la
poste et on reçoit un profil de risques – valait 200 dollars. Il coûte
aujourd’hui 99 dollars. Il y a déjà quelques applications concrètes de la
médecine prédictive, mais elles sont très peu nombreuses en pratique
quotidienne : le test des gènes prédisposant au cancer du sein
héréditaire, le test du gène prédisposant à une réaction médicamenteuse
mortelle chez certains malades du sida. Pour les maladies plurifactorielles
(maladies cardiaques, neurologiques, diabète…) combinant plusieurs gènes et
l’interaction avec l’environnement, beaucoup de scientifiques considèrent que
la médecine prédictive restera du domaine de l’illusion.
Quel sera l’intérêt majeur de cette nouvelle médecine ?
Il y en aurait de multiples mais, s’il faut n’en sélectionner qu’un,
disons que la façon dont on envisage le soin aujourd’hui dans notre pays serait
révolutionnée. Nous sommes dans un système curatif, la médecine prédictive
obligerait les patients, les médecins, la Sécurité sociale à s’orienter dans
une démarche préventive.
Pourrait-elle être détournée de ses fins sanitaires ?
Peut-être. Aujourd’hui, nous adhérons au système de soins et de
protection sociale parce que nous ne savons pas si nous allons vraiment tomber
malade et devoir un jour aller à l’hôpital, donc nous cotisons solidairement.
Si nous savons, le système de solidarité risque de ne plus tenir. La
détermination de risque de santé pourrait aussi intéresser les employeurs, pour
sélection à l’embauche ou pour gérer leurs ressources humaines. Mais ce ne sont
que des hypothèses. Encore faut-il que les multiples incertitudes scientifiques
soient levées et que le public adhère ■ PROPOS
RECUEILIS PAR JÉRÓME VINCENT
* Coauteur de
« Médecine prédictive : les balbutiements d’un concept aux enjeux
considérables », note d’analyse du CGSP, octobre 2012.

|
Décryptage. Sergey Brin et Anne Wojcicki, créatrice de
23andMe, en avril. |
Sergey Brin, futur tycoon de la
génétique ?
Croisade.
Le cofondateur de Google investit en masse pour déjouer la maladie.
PAR GUILLAUME GRAILLET
|
F |
aire reculer la mort. Jusqu’à la voir disparaître ? Il y a un
mois, Google lançait une nouvelle société : Calico. Son nom est une
contraction de California Life Company, mais c’est aussi le nom d’une ancienne
vile-fantôme du désert des Mojaves, haut lieu des chercheurs de minerais à la
fin du XIXe siècle, et qui revit aujourd’hui grâce à l’arrivée des
nouveaux habitants. Calico s’attachera notamment à lutter contre
« la moindre mobilité et l’agilité intellectuelle qui diminue avec
l’âge », à l’instar d’iPierian – spécialisée dans la lutte contre la
maladie d’Alzheimer – une autre société dans laquelle Google Ventures a pris
des participations.
Sergey Brin, le cofondateur de Google, a joué
un rôle clé dans ces investissements.
Ce fils d’un mathématicien, né il y a quarante ans dans le Moscou soviétique de
Brejnev, qui a rejoint les Etats-Unis à l’âge de 6 ans, est persuadé qu’il peut
une nouvelle fois changer le cours de sa vie. Le déclic remonte à 2006
lorsqu’il avais appris qu’il avait une probabilité située entre 30 et 75 % de
contracter un jour la maladie de Parkinson, dont souffre sa mère. Et ce grâce à
l’analyse ADN conduite par 23andMe.com, le site que venait de lancer Anne
Wojcicki, alors sa fiancée, une diplômée en biologie de l’université de Yale. « Depuis,
il vit la présence du gène LRRK2 comme un bug dans son code personnel et est
prêt à tout pour changer la donne », explique un proche. Cela passe
par l’exercice intensif de la plongée ou par la pratique du vélo sur les
chemins vallonnées de Santa Hill Road – « l’exercice peut faire baisser
la proportion de risque de moitié », explique-t-il au journal Wired.
Ou encore par l’investissement que fait Google dans la société 23andMe.com.
Car qui d’autre que Google peut s’affirmer
dans la médecine prédictive ? La firme née en 1998 dispose à la fois de
cash, mais surtout d’une capacité sans pareille de jongler avec les bases de
données. C’est son analyse fine des renvois hypertextes entre les différents
sites Internet qui nous pousse à l’utiliser chaque jour pour nos recherches en
ligne.
Or décrypter son code génétique est devenu le dernier hobby à la mode chez les
Américains : plus de 500 000 l’ont fait ces deux dernières années, en
échange d’un chèque de 99 dollars. Résultat : ajoutées aux capteurs
d’activité qui se multiplient, jamais des informations personnelles numérisées
n’ont été disponibles en si grande quantité, ce qui permet de croiser
itinéraires de vie et risques comme jamais auparavant. Du coup, tout
deviendrait prévisible !
« Moonshot ». L’adepte de yoga qu’est Sergey Brin investit
par ailleurs dans une foule de projets baptisés « Moonshot »,
c’est-à-dire censés changer la vie à long terme, comme les voitures sans
conducteur qui devraient limiter les accidents, ou les Google Glass qui,
utilisés par les chirurgiens en Espagne ou à Chennai, en Inde, permettent
d’améliorer considérablement le déroulement d’une opération. L’entrepreneur a
par ailleurs récemment investi dans un projet visant à créer des steaks en
laboratoire. S’ils le pouvaient,
les bovidés applaudiraient des deux mains !
Croiser l’électronique et la biologie peut
donner naissance à des progrès fantastiques. IBM l’a bien compris en mettant
son super calculateur Watson à la disposition de chercheurs du monde entier,
tout comme le cocréateur de Microsoft Paul Allen a investi un demi-milliard de
dollars dans la recherche sur le cerveau. Il y a huit mois, pour montrer sa
détermination , Sergey Brin a participé au recrutement de Ray Kurzweil, qui
travaillera sur les interactions homme-machine, dans le langage notamment. Avec
le croisement de la neuroscience et de prothèses reproduites grâce à
l’impression 3D, ce dernier – âgé de
65 ans – est persuadé que, d’ici à dix ans, un être humain aura les capacités
de vivre jusqu’à 600 ans. Pas encore KO la mort, donc, mais sérieusement bousculée
■







